引言|從「合規」走向「能否被解釋」的關鍵轉向
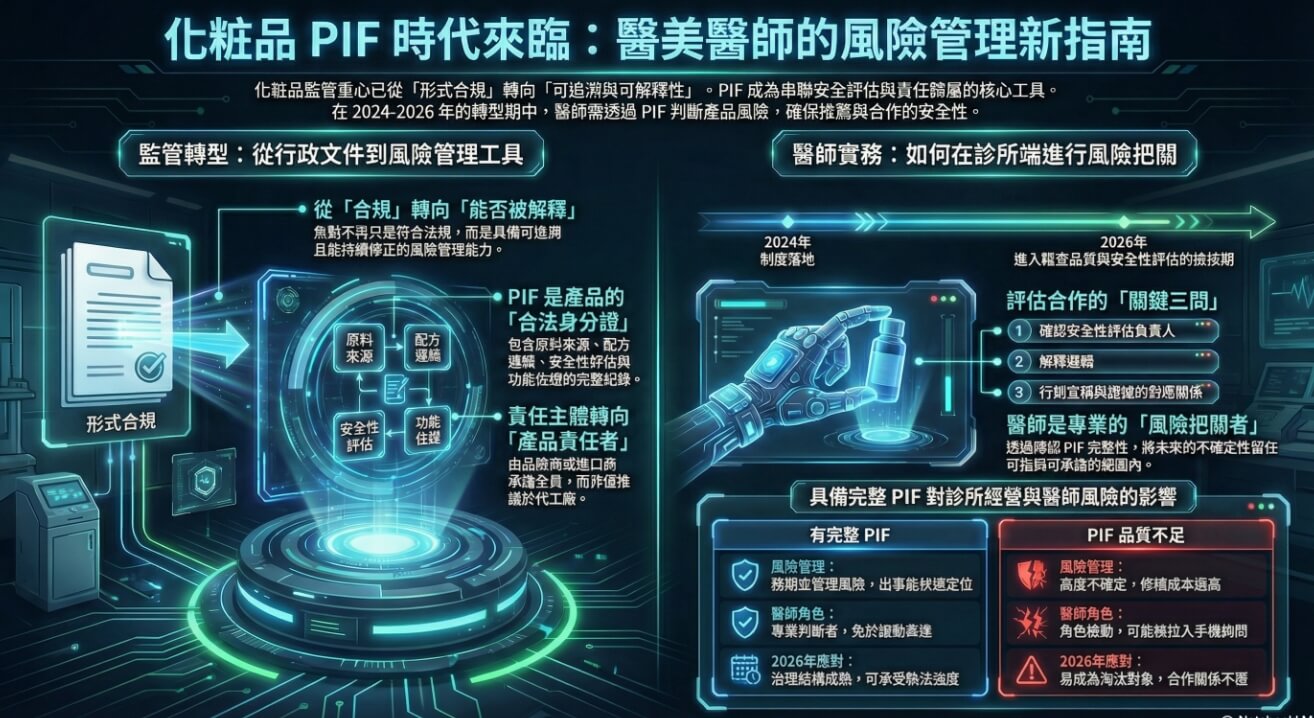
近五年的國際回顧顯示,化粧品監管的重心正在悄悄改變。焦點不再只是「是否符合法規」,而是是否具備一套能被追溯、被解釋、並在上市後持續修正的風險管理能力(註1、註2)。在這個轉向中,化粧品產品資訊檔案(PIF)被重新定位——它不只是備查文件,而是串聯安全性評估、責任歸屬與上市後監測的核心節點。
多數人的直覺,仍把化粧品視為低風險產品;但制度真正關心的盲點在於,長期使用、脆弱族群與行銷宣稱如何被放進同一套可說明的邏輯。當監管要求「說得清楚」,責任就不再只看角色名稱,而看誰能提出完整、安全且可回溯的論證。這也解釋了為什麼在 2024–2026 的治理轉型期,PIF 會從品牌端的行政工具,逐步影響到醫師在推薦、合作與判斷風險時的決策方式。
接下來,我們將沿著這條制度路線圖,整理這場轉型對醫師實務判斷的實際意義:哪些地方正在被重新檢視、哪些責任正在被放大、又有哪些問題值得你現在就先看懂。
化粧品 PIF 是什麼?為什麼現在醫師開始需要關心
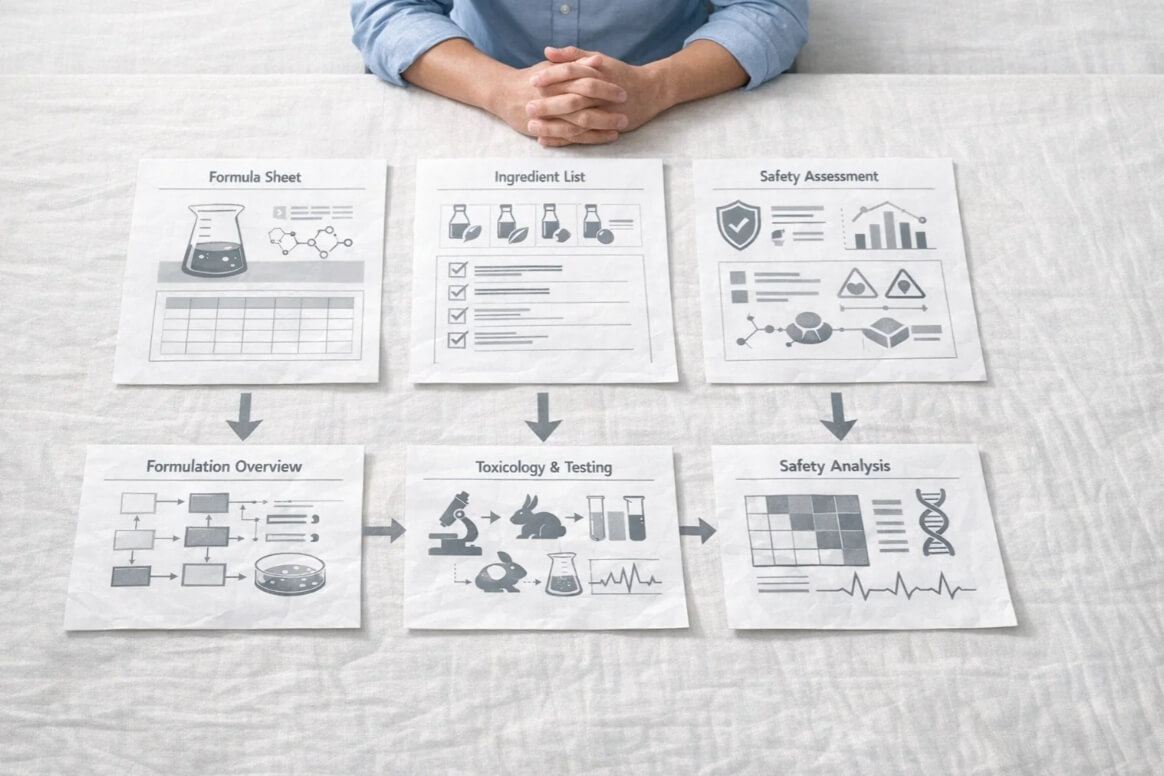
你有沒有發現,這一兩年,化粧品 PIF突然從「品牌端的文件」變成醫師圈開始討論的關鍵字?別小看這個轉變。PIF(Product Information File)其實就像每一件化粧品的「健康與合法身分證」,裡面不是行銷故事,而是原料來源、配方邏輯、安全性評估與功能佐證的完整紀錄。過去的監管模式偏向「事前登錄、形式合規」,但現在已明確轉向「事後稽查、責任自負」,這也是為什麼醫師推薦化粧品、評估診所合作時,開始不能只看成分表漂亮不漂亮。
如果用料理來比喻,PIF 就不是菜單,而是後廚的備料表與衛生紀錄。菜端上桌好不好吃很重要,但真正決定能不能過稽查的,是你有沒有交代清楚「這道菜為什麼這樣煮是安全的」。在現行制度下,化粧品安全責任被要求可追溯、可解釋,這讓 PIF 從「行政文件」升級為「風險管理工具」。對醫師而言,關鍵不在於你要不要親手寫 PIF,而是你是否意識到:當產品進入推薦、合作或販售情境,這份文件會直接影響責任邊界的判斷。
需要提醒的是,PIF 並不是萬能護身符。即便文件齊全,若安全性評估只是模板拼貼、缺乏實際暴露量與風險計算,仍可能在稽查時被視為無效。近年的國際回顧研究也指出,化粧品監管已越來越重視「結構化風險管理」與「上市後監測」,而非單點式的合規檢查(註1、註2)。這正是為什麼現在開始理解 PIF,對醫師來說不是多做功課,而是少踩一個未來會放大的坑。

醫師推薦化粧品,需要看 PIF 嗎?
你可能會問:「我只是推薦,不是製造商,真的需要看 PIF 嗎?」關鍵不在「需不需要親手處理文件」,而在於風險是否會被連動檢視。在 2024–2026 的治理轉型下,監管邏輯已從「形式合規」轉為「可追溯、可解釋」。一旦產品進入推薦、合作或診所販售情境,PIF 會成為判斷化粧品安全責任與風險歸屬的重要參考點。別小看這一點——你不看 PIF,不代表事件發生時不會被問到。
換個生活比喻。你邀請病人到家裡吃飯,未必親自下廚,但你會確認食材來源與保存狀況;因為一旦出現問題,「我只是介紹而已」往往不是能讓人安心的答案。同樣地,PIF 讓你快速判斷:品牌是否掌握配方主控權?安全性評估是否有人簽名、能說清暴露量與風險?行銷宣稱是否有對應佐證?這些不是行政瑣事,而是醫師是否把風險留在可控範圍的關鍵。
當然,也要避免另一個誤區:把「看 PIF」誤解成「背法規」。實務上,你要的是判斷工具而非專家身分。國際回顧顯示,現代化的化粧品治理強調結構化風險管理與上市後監測(cosmetovigilance),而非單次審核(註3)。美國的制度亦將重點放在標示、製造與不良反應回報的責任鏈(註4)。因此,對醫師而言,看 PIF 是為了問對問題:資料在不在?邏輯通不通?出事時能不能即刻回溯。
PIF 制度下,化粧品安全責任算誰的?
你可能會直覺以為,風險應該落在代工廠;但在 PIF 制度裡,法規關注的不是「誰做」,而是「誰負責」。關鍵角色叫做「產品責任者」——也就是品牌商或進口商。這個設計的核心精神很清楚:責任必須集中、可追溯。因此,當稽查發生,不能再用「資料在工廠」來切割風險;能否即時拿出完整 PIF,才是判斷合規與否的分水嶺。
用一個更生活的比喻:代工廠像是中央廚房,負責烹調;品牌則是開店的人,對外承擔一切。菜好不好吃是廚房的功,但出問題時找的是店家。在化粧品安全責任的邏輯中也是如此——品牌若未掌握配方比例、原料限制與安全性評估的解釋權,就等於把方向盤交出去,卻仍要對事故負全責。這也是為什麼 PIF 的重點不在「文件齊不齊」,而在「安全性評估是否由具資格的人完成、能否說清楚 NOAEL、暴露量與 MoS 的計算邏輯」。
需要提醒的是,責任集中並不代表監管單向。近年的綜述指出,現代化妝品治理正在把重心放在整體風險治理:從配方設計、毒理評估,到上市後的不良反應回報與修正(註5)。當品牌把責任外包、醫師把判斷外包,制度留下的縫隙就會被放大(註6)。因此,理解「責任落點」不是找戰犯,而是把風險留在可管理的框架內。
2024–2026 法規時程,醫師現在要注意什麼
你可能會想:「等到全面上路再說,會不會比較省力?」小心,這正是最容易誤判的地方。2024–2026 的分階段時程,表面看是寬限,實際上是把市場從「有沒有做」推進到「做得真不真」。2024 是起跑點,讓制度落地;2026 則是品質檢核期,稽查焦點會轉向安全性評估是否完整、是否能被解釋、是否能即時回溯。別小看這一點——等到 2026 才補文件,往往補的是形式,不是邏輯。
換個比喻。這像是一場長跑:前兩年裁判提醒你「記得穿鞋」,第三年開始檢查你是不是真的能跑完全程。在化粧品 PIF 的節奏裡,醫師現在要做的不是趕進度,而是提前看懂結構:品牌是否把配方主控權握在手裡?安全性評估是否由具資格者完成並簽名?上市後監測是否有流程?這些都會在執法成熟期被放大檢視。
需要注意的是,國際趨勢已把重心放在上市後監測與真實世界資料,而非一次性的合規(註7、註8)。這意味著,醫師越早用 PIF 來判斷品牌的風險治理能力,越能把不確定性留在可控範圍。現在準備,不是多做功課;而是避免在成熟期被動承擔後果。
結論|把責任留在可承擔的地方
制度的轉變,從來不是為了增加負擔,而是讓風險回到能被整理的位置。2024–2026 的化粧品 PIF 治理轉型,說穿了只是在問一件事:當問題發生時,你能不能說清楚為什麼這樣做是安全的。這不是挑戰專業,而是考驗準備。
後世醫家在解讀《黃帝內經》時常提醒,醫道不只在治已病,更在於未亂先整。把這個精神放進制度裡,PIF 的角色就很清楚了——它不是為了檢查而存在,而是讓責任、邏輯與證據能彼此對齊。就像開方配伍,再好的藥材,若劑量與脈絡說不清,反而成了風險。
你現在其實可以做兩件很實際的事。
第一,當評估品牌合作或診所引進品項時,直接問一句:「這份產品的安全評估,誰負責?誰能解釋?」如果答案模糊,風險也會跟著模糊。
第二,面對行銷宣稱,不必急著判斷效果,而是回頭確認:「這個說法,在 PIF 裡對應的是哪一段證據?」問對問題,往往比記住條文更重要。
多數人忽略的,是制度真正要改變的並不是文件,而是思考方式;再往深一層看,這場轉型其實是在把「你敢不敢為這個選擇負責」攤在檯面上。醫者的角色,從來不是站在最前面賣力推廣,而是在關鍵時刻替人把關。
所以,別等到 2026 才開始緊張。現在多看懂一點結構、多問一句關鍵問題,就是把未來的不確定,留在自己能承擔的範圍裡。
如果你在實務上遇到模糊地帶或想釐清的情境,歡迎留下你的問題——《本文將依據最新提問持續更新》。
| 比較面向 | 有完整、可解釋的 PIF | 沒有 PIF/PIF 品質不足 |
|---|---|---|
| 風險暴露程度 | 風險可預期、可管理。問題發生時,能快速定位來源與責任節點。 | 風險高度不確定,事件往往在發生後才被看見,修補成本高。 |
| 責任歸屬清晰度 | 產品責任者明確,安全性評估與資料保存有跡可循,不易產生模糊地帶。 | 常出現「資料在工廠」「還在補文件」等灰色說法,責任邊界模糊。 |
| 稽查或爭議時的應對能力 | 可即時提出完整資料與安全評估邏輯,降低事件升級與外溢風險。 | 難以即時提出完整解釋,容易被認定為制度失靈或管理不足。 |
| 行銷宣稱的反噬風險 | 宣稱與佐證可對應,較不容易因過度包裝而被放大檢視。 | 宣稱寫得越滿,技術資料越撐不住,風險被放大檢視的機率越高。 |
| 對醫師角色的實際影響 | 醫師能站在「專業判斷者」位置,而非被動被牽連的關係人。 | 醫師可能從推薦者被拉進「為何沒確認」的詢問範圍,角色被動。 |
| 長期合作的穩定性 | 治理結構成熟,較能承受 2026 年後的執法強度與制度檢核。 | 在執法成熟期容易成為淘汰對象,合作關係不穩定。 |
常見問題與回覆
問題1:醫師只是推薦化粧品,真的需要在意 PIF 嗎?
回覆:需要在意,但不代表你要親自處理文件。重點不在「會不會被要求拿出 PIF」,而在於當發生爭議時,你能不能判斷這個產品是否站在一個合理、安全的制度基礎上。把 PIF 當成判斷工具,而不是行政負擔,會讓你更安心。
問題2:PIF 不是品牌或代工廠的事嗎?責任真的會影響到醫師嗎?
回覆:法律責任主要在產品責任者,但實務上,醫師的專業角色常會被連動詢問「是否有合理確認」。當資料模糊、說不清楚時,風險就容易外溢。理解制度,不是替品牌背責任,而是避免自己站在被動的位置。
問題3:如果品牌說 PIF 都有準備好,但不方便提供,這樣可以接受嗎?
回覆:這是一個需要提高警覺的訊號。你不一定要看到全部細節,但至少要確認「誰負責安全性評估」、「能不能解釋評估邏輯」。如果連基本輪廓都說不清,往往代表制度成熟度不足,合作風險自然偏高。
問題4:等到 2026 全面上路再來看 PIF,會不會比較實際?
回覆:這是很多人直覺會做的選擇,但風險反而更高。前期是建立結構的時間,後期才是品質被檢核的階段。太晚開始,常常補的是形式,而不是能被解釋的邏輯。提早看懂結構,比趕進度更重要。
問題5:醫師不想碰法規,有沒有一個比較輕鬆的判斷方式?
回覆:有的,你可以先練習問三個問題:這個產品的安全評估誰負責?出了問題誰能解釋?行銷說法和資料是否對得起來?不用懂條文,也能快速判斷這是不是一個值得信任的合作對象。這樣的做法,其實很符合「先整理、再出手」的養生思維。
本文作者:GCM上醫預防醫學發展協會 數位編輯部
總編輯:草本上膳醫廚-黃子彥
免責聲明:本文所提供之信息僅供參考,並非醫療建議,無特定商業合作關係,亦無針對特定商品進行推薦。在進行任何飲食或健康改變前,請先咨詢專業醫師或營養師。
參考文獻:
- Arnesdotter, E., Rogiers, V., Vanhaecke, T., & Vinken, M. (2021). An overview of current practices for regulatory risk assessment with lessons learnt from cosmetics in the European Union. Critical Reviews in Toxicology, 51(7), 595–614. DOI: 10.1080/10408444.2021.1954959
- SCCS. (2021). Notes of Guidance for the Testing of Cosmetic Ingredients and Their Safety Evaluation, 11th Revision. Regulatory Toxicology and Pharmacology, 123, 104958. DOI: 10.1016/j.yrtph.2021.104958
- Ribet, V., Albinet Claudin, L., Brinio, E., et al. (2021). Surveillance of dermo-cosmetic products: A global cosmetovigilance system to optimise product development and consumer safety. European Journal of Dermatology, 31(5), 594–603. DOI: 10.1684/ejd.2021.4096
- Katz, L. M., Lewis, K. M., Spence, S., & Sadrieh, N. (2022). Regulation of cosmetics in the United States. Dermatologic Clinics, 40(3), 303–314. DOI: 10.1016/j.det.2022.02.004
- Arnesdotter, E., Rogiers, V., Vanhaecke, T., & Vinken, M. (2021). An overview of current practices for regulatory risk assessment with lessons learnt from cosmetics in the European Union. Critical Reviews in Toxicology, 51(7), 595–614. DOI: 10.1080/10408444.2021.1954959
- Thakur, M., & Bala, R. (2025). Challenges and opportunities of cosmeceutical regulations: A global perspective. International Journal of Toxicology, 44(1), 3–15. DOI: 10.1177/1091581824123456
- Aljallal, M. A., Alhumaid, M. I., Alkathiri, F. A. (2025). Evaluating reporting trends and adverse effects of cosmetic products based on cosmovigilance data. Scientific Reports, 15, 12345. DOI: 10.1038/s41598-025-12345-6
- Mehta, G., Tyagi, D. R., Sachdeva, M., et al. (2024). An observational study on cosmetics use-related adverse effects: Cosmetovigilance need of the day. Drug Research, 74(6), 301–308. DOI: 10.1055/a-2123-4567